カレントテラピー 35-9 サンプル page 24/34
このページは カレントテラピー 35-9 サンプル の電子ブックに掲載されている24ページの概要です。
秒後に電子ブックの対象ページへ移動します。
「電子ブックを開く」をクリックすると今すぐ対象ページへ移動します。
概要:
カレントテラピー 35-9 サンプル
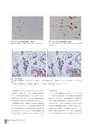
72 Current Therapy 2017 Vol.35 No.9886染色強度については,ERにおけるAllred scoreなどとは異なり,評価しない.しかし,自動染色装置を用いても,核の染色性に濃淡を生じることが多いため,再現性を得るためには少しでもDABの発色が確認されれば陽性核と判断するのが現実的と思われる.計測個数は500個,1,000個,2,000個など個数を定めて行われることが多い.平均的な部位を採用する場合には判定個数が多いほど信頼性が高い結果が得られると思われるが,hot spot法では多数の細胞を計測すればするほど,平均値に近づきLIが下がってゆく可能性がある.カウントは,顕微鏡下での目視と,プリントアウトして計測する方法がある.前者は慣れれば比較的簡便に行うことができる.後者は印刷などの手間がかかるが,計測の記録が残るため,振り返りには向いているかもしれない.安定した計測を行うためには,選んだ視野の浸潤癌細胞を漏れなく順番に計測することが推奨される(図3)9).より簡便な方法として,半定量的な計測法も提唱されている.必ずしも絶対的なカットオフ値が設定されていない現状においては,病図2 Ki 67 に対する免疫組織染色(強拡大)少しでも核に発色が見られれば陽性と判定する(矢印).染色強度は考慮しない.図1 Ki 67 に対する免疫組織染色(弱拡大)浸潤癌成分を評価する.腫瘍内の染色性は必ずしも均質ではない.13 9 8 7 6 5 4 3 21101112a) b)図3 Ki 67 の計測法定めた視野の浸潤癌細胞を,一定の方法ですべて評価する.合計の判定個数を決めて(1,000 個など)行う.H -E とも対比し,リンパ球などは除外する.a:染色標本:浸潤癌成分を*,非浸潤癌成分を◆で示す.b:計測手順:実際には細胞を一列ずつカウントしていく.